Fecha de publicación: 8 de Enero de 2026 a las 17:23:00 hs
Medio: INFOBAE
Categoría: GENERAL
Cómo funciona la innovadora terapia con células madre que podría revertir secuelas físicas tras un ACV
Descripción: Investigadores internacionales descubrieron un mecanismo genético capaz de guiar nuevas neuronas para que ocupen áreas lesionadas del sistema nervioso. Las claves de un descubrimiento que impulsa avances en la medicina regenerativa y la rehabilitación neurológica avanzada
Contenido: Las terapias con células madre representan una nueva perspectiva en el tratamiento del accidente cerebrovascular (ACV), una de las principales causas de discapacidad en todo el mundo.
Investigadores del Sanford Burnham Prebys Medical Discovery Institute, en colaboración con la Duke-National University of Singapore (NUS) Medical School, comprobaron que células humanas trasplantadas en el cerebro de ratones pueden sobrevivir, madurar y reconstruir circuitos neuronales, lo que permite restaurar funciones motoras perdidas.
Este avance, realizado en modelos animales y publicado en la revista Cell Stem Cell, revela el mecanismo que orienta a las células hacia su ubicación en el tejido cerebral dañado y consolida un progreso relevante para la medicina regenerativa.
Un accidente cerebrovascular, en este caso el identificado como isquémico (es decir, que el que ocurre cuando un vaso —vena o arteria— se obstruye), ocurre cuando se interrumpe el flujo sanguíneo hacia una parte del cerebro. Esto provoca la muerte de células cerebrales y deja secuelas motoras, cognitivas y sensoriales. El entorno del cerebro adulto, tras este tipo de lesión, se convierte en un espacio desfavorable para la regeneración celular.
Según Sanford Burnham Prebys, predominan moléculas inflamatorias y tejido cicatricial, que dificultan la integración de nuevas células terapéuticas. Su-Chun Zhang, director del Centro de Enfermedades Neurológicas del instituto, explicó: “En el cerebro adulto, tras un ACV, el entorno es hostil y las células deben sobrevivir en una especie de pantano peligroso”.
Para avanzar en el trasplante de células madre, la investigación se enfocó en superar los obstáculos que impiden que las nuevas células se integren en la zona lesionada. El equipo utilizó una combinación de fármacos y proteínas estructurales.
Así, las células lograron resistir el entorno adverso, ocupar la región dañada y sentar las bases para la reconstrucción funcional del tejido. El siguiente desafío era establecer si esas neuronas podrían atravesar el tejido cicatricial y restablecer conexiones activas.
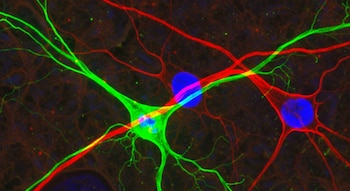
En los experimentos realizados, los científicos confirmaron que las células trasplantadas maduraron y se integraron en circuitos cerebrales clave, como la corteza cerebral y la vía corticoespinal. Tras el trasplante en ratones, las neuronas formaron conexiones específicas con otras regiones cerebrales y permitieron la recuperación de funciones motoras previamente afectadas por el accidente cerebrovascular.
El avance crucial de este trabajo reside en el descubrimiento de un código genético de orientación o “código transcripcional para la orientación axonal”, que guía a las células trasplantadas hasta su destino en el cerebro dañado.
Este código determina cómo cada tipo celular dirige sus axones para conectarse con áreas concretas del cerebro y la médula espinal. Zhang señaló: “Descubrimos que los distintos tipos neuronales trasplantados encuentran a sus propios socios incluso en el contexto complejo del cerebro adulto”.
¿Qué es un axón y por qué es importante su orientación? El axón es una prolongación de la neurona responsable de transmitir impulsos eléctricos hacia otras células del sistema nervioso. La capacidad de los axones para orientarse y reconectar regiones cerebrales dañadas resulta esencial en la recuperación de funciones tras un accidente cerebrovascular.
La publicación en Cell Stem Cell destaca que existen subtipos neuronales con patrones de conexión característicos, guiados por factores genéticos que regulan la dirección y la integración en los circuitos afectados.
El equipo utilizó aprendizaje automático para identificar estos subtipos y analizar cómo la presencia o ausencia de proteínas como Ctip2 modificaba el destino de las conexiones formadas. Comprender estos mecanismos permitirá seleccionar los subtipos neuronales más adecuados para estrategias futuras de reparación cerebral.
Estos resultados respaldan un enfoque más preciso y personalizado en las terapias regenerativas. Sanford Burnham Prebys subraya la importancia de entender cómo se integran y orientan las células trasplantadas, lo que hará posible diseñar tratamientos efectivos en humanos para restaurar circuitos neuronales dañados por accidentes cerebrovasculares y otras enfermedades neurológicas.
Este avance sienta nuevas bases científicas para el abordaje de lesiones cerebrales graves y fortalece las expectativas de que las terapias celulares puedan beneficiar a millones de personas en el futuro. La medicina regenerativa se consolida como una esperanza tangible frente a los desafíos del daño cerebral permanente.
Imágenes adicionales



Visitas: 0